Korosi (Perkaratan) merupakan reaksi redoks spontan antar logam dengan zat yang ada di sekitarnya dan menghasilkan senyawa yang tidak dikehendaki biasanya berupa oksida logam atau logam karbonat. Korosi terjadi karena sebagian besar logam mudah teroksidasi dengan melepas oksigen di udara dan membentuk oksida logam. Mudah tidaknya suatu logam terkorosi dapat dipahami dari deret Volta ataupun nilai potensial elektrode standarnya, Eo.
Sebagai contoh, logam besi (Fe) dengan potensial elektrode sebesar -0,44 lebih mudah terkorosi dibandingkan dengan logam emas yang memiliki potensial elektrode standar Eo sebesar +1,50.
Secara umum korosi logam melibatkan beberapa reaksi sebagai berikut:
1. Reaksi oksidasi logam pada anode:
L → L n+ + ne–
2. Reaksi reduksi pada katode yang mungkin terjadi adalah:
• Reduksi O2 menjadi ion OH– (kondisi netral atau basa)
O2(aq) + H2O(I) + 2e– → 2OH–(aq)
• Reduksi O2menjadi H2O (kondisi asam)
O2(aq) + 4H+(aq) + 4e– → 2H2O(I)
• Evolusi/Pembentukan H2
2H+(aq) + 2e– → H2(g)
• Reduksi Ion Logam
L3+(aq) + e– → L2+(aq)
• Deposisi Logam
L+(aq) + e– → L(s)
Perbandingan logam yang Belum Terkorosi (kiri) Dengan yang Telah Terkorosi
Berikut contoh reaksi korosi yang terjadi pada logam besi.
Reaksi Korosi pada Besi
Pada kondisi netral atau basa, ion Fe2+ dan OH– selanjutnya membentuk endapan Fe(OH)2. Di udara, Fe(OH)2 tidak stabil dan membenrtuk Fe2O3 xH2O. Inilah yang disebut karat. Pada kondisi asam, banyaknya ion H+ memicu terjadinya reaksi reduksi lainnya yang juga berlangsung, yakni evolusi atau oembentukan hidrogen menurut persamaan reaksi: 2H+(aq) + 2e– → H2(g). Adanya 2 reaksi di katode pada kondisi asam menyebabkan lebih banyak logam besi yang teroksidasi. Hal ini menjelaskan mengapa korosi paku besi pada kondisi asam lebih besar daripada korosi dalam air.
Faktor-Faktor Yang Mempengaruhi Korosi
Korosi pada permukaan suatu logam dapat dipercepat oleh beberapa faktor, antara lain:
1. Kontak Langsung logam dengan H2O dan O2
Korosi pada permukaan logam merupakan proses yang mengandung reaksi redoks. Reaksi yang terjadi ini merupakan sel Volta mini. sebagai contoh, korosi besi terjadi apabila ada oksigen (O2) dan air (H2O). Logam besi tidaklah murni, melainkan mengandung campuran karbon yang menyebar secara tidak merata dalam logam tersebut. Hal tersebut menimbulkan perbedaan potensial listrik antara atom logam dengan atom karbon (C). Atom logam besi (Fe) bertindak sebagai anode dan atom C sebagai katode. Oksigen dari udara yang larut dalam air akan tereduksi, sedangkan air sendiri berfungsi sebagai media tempat berlangsungnya reaksi redoks pada peristiwa korosi. Jika jumlah O2 dan H2O yang mengalami kontak dengan permukaan logam semakin banyak, maka semakin cepat berlangsungnya korosi pada permukaan logam tersebut.
2. Keberadaan Zat Pengotor
Zat Pengotor di permukaan logam dapat menyebabkan terjadinya reaksi reduksi tambahan sehingga lebih banyak atom logam yang teroksidasi. Sebagai contoh, adanya tumpukan debu karbon dari hasil pembakaran BBM pada permukaan logam mampu mempercepat reaksi reduksi gas oksigen pada permukaan logam yang mengakibatkan proses korosi semakin cepat pula.
Pengotor yang Mempercepat Korosi pada Permukaan Logam
3. Kontak dengan Elektrolit
Keberadaan elektrolit, seperti garam dalam air laut dapat mempercepat laju korosi dengan menambah terjadinya reaksi tambahan. Konsentrasi elektrolit yang besar dapat meningkatkan laju aliran elektron sehingga laju korosi meningkat.
Bangkai Kapal di Dasar Laut yang Telah Terkorosi oleh Kandungan Garam yang Tinggi
4. Temperatur
Temperatur mempengaruhi kecepatan reaksi redoks pada peristiwa korosi. Secara umum, semakin tinggi temperatur maka semakin cepat terjadinya korosi. Hal ini disebabkan dengan meningkatnya temperatur maka meningkat pula energi kinetik partikel sehingga kemungkinan terjadinya tumbukan efektif pada reaksi redoks semakin besar dan laju korosi pada logam semakin meningkat. Efek korosi yang disebabkan oleh pengaruh temperatur dapat dilihat pada perkakas-perkakas atau mesin-mesin yang dalam pemakaiannya menimbulkan panas akibat gesekan (seperti cutting tools ) atau dikenai panas secara langsung (seperti mesin kendaraan bermotor).
Knalpot Kendaraan Bermotor yang Mudah Terkorosi Akibat Temperatur Tinggi
5. pH
Peristiwa korosi pada kondisi asam, yakni pada kondisi pH < 7 semakin besar, karena adanya reaksi reduksi tambahan yang berlangsung pada katode yaitu:
2H+(aq) + 2e– → H2
Adanya reaksi reduksi tambahan pada katode menyebabkan lebih banyak atom logam yang teroksidasi sehingga laju korosi pada permukaan logam semakin besar.
Korosi Pada Kondisi Asam Lebih Cepat Terjadi (atas). Logam Besi yang Belum Terkorosi Pada Kondisi Netral (bawah)
6. Metalurgi
- Permukaan logam
Permukaan logam yang lebih kasar akan menimbulkan beda potensial dan memiliki kecenderungan untuk menjadi anode yang terkorosi.
Permukaan Logam yang Kasar Cenderung Mengalami Korosi
- Efek Galvanic Coupling
Kemurnian logam yang rendah mengindikasikan banyaknya atom-atom unsur lain yang terdapat pada logam tersebut sehingga memicu terjadinya efek Galvanic Coupling , yakni timbulnya perbedaan potensial pada permukaan logam akibat perbedaan E° antara atom-atom unsur logam yang berbeda dan terdapat pada permukaan logam dengan kemurnian rendah. Efek ini memicu korosi pada permukaan logam melalui peningkatan reaksi oksidasi pada daerah anode.
7. Mikroba
Adanya koloni mikroba pada permukaan logam dapat menyebabkan peningkatan korosi pada logam. Hal ini disebabkan karena mikroba tersebut mampu mendegradasi logam melalui reaksi redoks untuk memperoleh energi bagi keberlangsungan hidupnya. Mikroba yang mampu menyebabkan korosi, antara lain: protozoa, bakteri besi mangan oksida, bakteri reduksi sulfat, dan bakteri oksidasi sulfur-sulfida. Thiobacillus thiooxidans Thiobacillus ferroxidans.
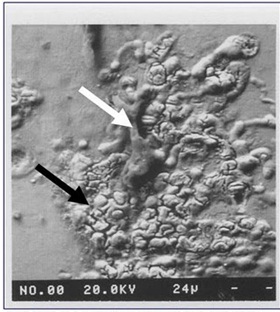
Korosi Pada Permukaan Logam yang Disebabkan oleh Mikroba
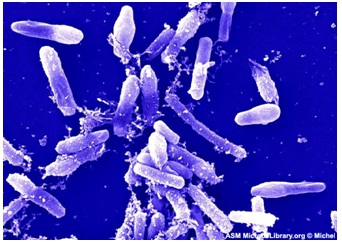
Koloni Bakteri Thiobacillus ferrooxidans Pada Permukaan Logam Besi yang Terkorosi
Koloni Bakteri Thiobacillus thiooxidans yang Dapat Menyebabkan Korosi Pada Logam
To be continued…..
(Ahmad Fathonah)
————————-mechanicalengboy.wordpress.com————————
Sumber :
“LAPORAN RESMI KERJA PRAKTEK PT. PUSRI PALEMBANG MAINTENANCE PADA CENTRIFUGAL PUMP P-III PLANT AMMONIA DAN UREA”
oleh Ahmad Fathonah, dosen pembimbing Ir. Suwarmin, PE (2011)








thx so much, Sir 🙂
sangat membantu tugas kimiaku 🙂
Pak korosi dengan asam kan lebih cepat
tadi bapak tuliskan pembentukan air di katode saat besi itubereaksi dg asam/basa..
knpa air??
dari mana pak?
It’s very good knowledge to common people like me.